Avtor:
Judy Howell
Datum Ustvarjanja:
27 Julij. 2021
Datum Posodobitve:
23 Junij 2024
Vsebina
- Stopati
- 1. del od 4: Razumevanje strukture
- 2. del od 4: Razumevanje simbola in poimenovanja
- 3. del od 4: Odčitavanje atomske številke
- 4. del od 4: Odčitavanje atomske mase
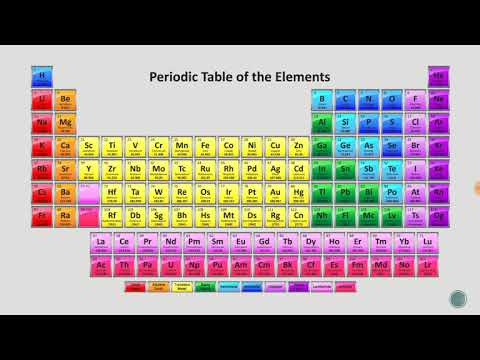
Periodična tabela elementov je seznam do zdaj odkritih 118 elementov. Obstaja več simbolov in številk, ki označujejo razlike v elementih, medtem ko je v strukturi tabele elementi razvrščeni glede na podobnosti. Periodični sistem lahko preberete po spodnjih smernicah.
Stopati
1. del od 4: Razumevanje strukture
 Periodični sistem si oglejte tako, kot da se začne zgoraj levo in konča na koncu zadnje vrstice, spodaj in desno. Tabela je strukturirana od leve proti desni po naraščajočem atomskem številu. Atomsko število je število protonov v posameznem atomu.
Periodični sistem si oglejte tako, kot da se začne zgoraj levo in konča na koncu zadnje vrstice, spodaj in desno. Tabela je strukturirana od leve proti desni po naraščajočem atomskem številu. Atomsko število je število protonov v posameznem atomu. - Vsaka vrstica ali stolpec ni popoln. Čeprav so v sredini vrzeli, še naprej prebirajte tabelo od leve proti desni. Na primer, vodik ima atomsko številko 1 in se nahaja v zgornjem levem kotu. Helij ima atomsko številko 2 in je v zgornjem desnem kotu.
- Elementi od 57 do 71 so ponavadi prikazani kot podmnožica v spodnjem desnem kotu tabele. To so "elementi redke zemlje".
 V vsakem stolpcu tabele boste našli "skupino" elementov. Obstaja 18 stolpcev.
V vsakem stolpcu tabele boste našli "skupino" elementov. Obstaja 18 stolpcev. - Za branje od zgoraj navzdol uporabite izraz "branje skupine".
- Oštevilčenje je običajno navedeno nad stolpci; lahko pa je tudi v drugih skupinah, kot so kovine.
- Številčenje, kot se uporablja v periodnem sistemu, se zelo razlikuje. Lahko so rimski (IA), arabski (1A) ali številke od 1 do 18.
- Vodik je lahko v družini halogenov in alkalijskih kovin ali oboje.
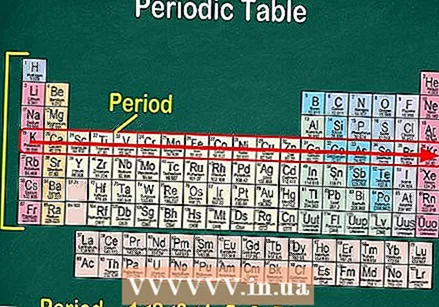 V vsaki vrstici tabele boste našli "obdobja" elementov. Obstaja 7 obdobij. Za branje od leve proti desni uporabite besedno zvezo »branje vzdolž pike«.
V vsaki vrstici tabele boste našli "obdobja" elementov. Obstaja 7 obdobij. Za branje od leve proti desni uporabite besedno zvezo »branje vzdolž pike«. - Obdobja so običajno oštevilčena od 1 do 7 na levi strani tabele.
- Vsako obdobje je večje od prejšnjega. To je povezano s povečanjem ravni energije atomov v periodnem sistemu.
 Razumevanje dodatnih skupin kovin, polkovin in nekovin. Barve se zelo razlikujejo.
Razumevanje dodatnih skupin kovin, polkovin in nekovin. Barve se zelo razlikujejo. - Skupina Kovine ima eno barvo. Vendar ima vodik pogosto enako barvo in skupino kot nekovine. Kovine imajo lesk, običajno so pri sobni temperaturi trdne, prevajajo toploto in elektriko ter so voljne in voljne.
- Nekovine imajo enako barvo. To so elementi od C-6 do Rn-86, vključno s H-1 (vodik). Nimajo sijaja, prevajajo toploto in elektriko in niso voljni. Običajno tvorijo plin pri sobni temperaturi in so lahko trdna snov, plin ali tekočina.
- Polkovine / metaloidi imajo običajno vijolično ali zeleno barvo kot kombinacijo drugih dveh barv. Črta je diagonalna in se razteza od elementov B-5 do At-85. Imajo nekatere lastnosti kovin in nekatere nekovine.
 Upoštevajte, da so elementi včasih navedeni tudi v družinah. To so alkalijske kovine (1A), zemeljskoalkalijske kovine (2A), halogeni (7A), žlahtni plini (8A) in ogljikovi atomi (4A).
Upoštevajte, da so elementi včasih navedeni tudi v družinah. To so alkalijske kovine (1A), zemeljskoalkalijske kovine (2A), halogeni (7A), žlahtni plini (8A) in ogljikovi atomi (4A). - Oštevilčenje je lahko rimsko, arabsko ali standardno število.
2. del od 4: Razumevanje simbola in poimenovanja
 Najprej preberite simbol. Sestavljen je iz ene ali dveh črk in je standarden v več jezikih.
Najprej preberite simbol. Sestavljen je iz ene ali dveh črk in je standarden v več jezikih. - Simbol je mogoče izpeljati iz latinskega imena elementa ali njegovega skupnega poimenovanja.
- V mnogih primerih simbol sledi angleški konvenciji o poimenovanju, na primer Helij ali "He". Vendar ni pravilo, ki bi ga lahko domnevali. Železo je na primer "Fe". Zaradi tega se kombinacija simbolov / imen običajno zapomni za hitro uporabo.
 Poglejte splošno ime. To je neposredno pod simbolom. To se razlikuje glede na jezik, v katerem je napisan periodni sistem.
Poglejte splošno ime. To je neposredno pod simbolom. To se razlikuje glede na jezik, v katerem je napisan periodni sistem.
3. del od 4: Odčitavanje atomske številke
 Preberite periodni sistem glede na atomsko številko v zgornjem središču polja vsakega elementa. Kot smo že omenili, je sistem razvrščen od zgoraj levo navzdol desno. Poznavanje atomske številke je najhitrejši način za iskanje več informacij o elementu.
Preberite periodni sistem glede na atomsko številko v zgornjem središču polja vsakega elementa. Kot smo že omenili, je sistem razvrščen od zgoraj levo navzdol desno. Poznavanje atomske številke je najhitrejši način za iskanje več informacij o elementu. 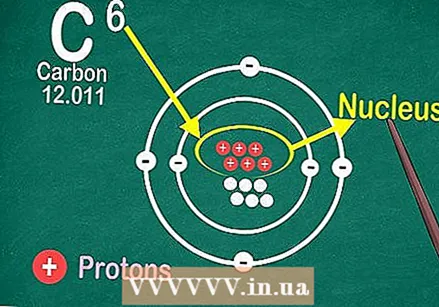 Atomsko število je število protonov v jedru posameznega atoma elementa.
Atomsko število je število protonov v jedru posameznega atoma elementa. Dodajanje ali odstranjevanje protonov ustvarja drugačen element.
Dodajanje ali odstranjevanje protonov ustvarja drugačen element. Ugotovitev števila protonov v atomu določa tudi število elektronov. Atomi imajo toliko elektronov kot protoni.
Ugotovitev števila protonov v atomu določa tudi število elektronov. Atomi imajo toliko elektronov kot protoni. - Upoštevajte, da je to pravilo izjema. Ko atom izgubi ali pridobi elektrone, postane električno nabit ion.
- Če je poleg simbola elementa znak plus, to pomeni, da je pozitivno napolnjen. S simbolom minus je negativno nabit.
- Če ni simbola plus ali minus in vaša težava s kemijo ni v zvezi z ioni, potem je število protonov in elektronov verjetno enako.
4. del od 4: Odčitavanje atomske mase
 Določite atomsko maso. To je številka pod splošnim imenom elementa.
Določite atomsko maso. To je številka pod splošnim imenom elementa. - Čeprav se zdi, da se atomska masa povečuje od zgornjega levega dela sistema do spodnjega desnega, to v vseh primerih ne drži.
 Razumejte, da je večina elementov predstavljena z decimalnimi mesti. Atomska masa je vsota delcev v jedru; vendar je tehtano povprečje različnih izotopov.
Razumejte, da je večina elementov predstavljena z decimalnimi mesti. Atomska masa je vsota delcev v jedru; vendar je tehtano povprečje različnih izotopov.  Z atomsko maso poiščite število nevtronov v posameznem atomu. Atomsko maso zaokroži na najbližje celo število, masno število. Nato od masnega števila odštejete število protonov, da določite število nevtronov.
Z atomsko maso poiščite število nevtronov v posameznem atomu. Atomsko maso zaokroži na najbližje celo število, masno število. Nato od masnega števila odštejete število protonov, da določite število nevtronov. - Na primer: Atomska masa železa je 55,847, torej je njegovo masno število 56. Element ima 26 protonov. 56 (masno število) minus 26 (protoni) je 30. V enem samem atomu železa je običajno 30 nevtronov.
- S spreminjanjem števila nevtronov v atomu nastanejo izotopi, ki so težja ali lažja različica atoma.



