Avtor:
Randy Alexander
Datum Ustvarjanja:
2 April 2021
Datum Posodobitve:
1 Julij. 2024

Vsebina
Kemijska enačba je simbolni prikaz kemijske reakcije. Reagenti so napisani na levi, izdelek pa na desni. Zakon o ohranjanju mase kaže, da se v kemijski reakciji ne rodi ali izgubi noben atom, zato mora biti število atomov, ki so prisotni v reaktantu, enako številu atomov, prisotnih v reakciji. izdelka. Po tej vadnici lahko uravnotežite kemijske enačbe na različne načine.
Koraki
Metoda 1 od 2: Ravnotežje po tradicionalni metodi
Napiši dano enačbo. V tem primeru bi imeli: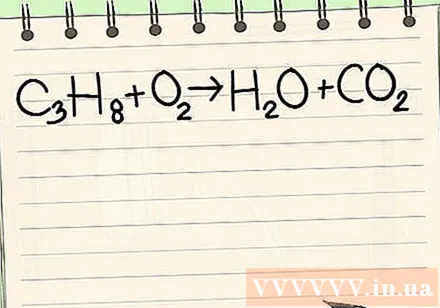
- C3H8 + O2 -> H2O + CO2
- Ta reakcija se pojavi, ko propan (C3H8zgoreli v kisiku, da nastanejo voda in ogljikov dioksid.

Zapišite število atomov za vsak element, ki ga imate na vsaki strani enačbe. Oglejte si spodnje indekse poleg vsakega atoma, da poiščete število atomov v enačbi.- Levo: 3 ogljika, 8 vodika in 2 kisika.
- Desno: 1 ogljik, 2 vodika in 3 kisika.
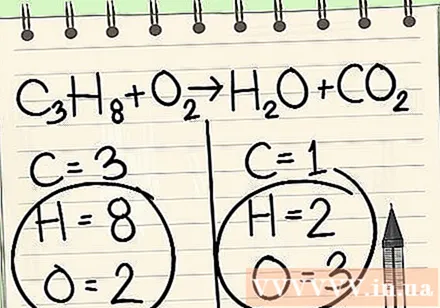
Na koncu vedno pustite vodik in kisik.
Če imate za uravnoteženje več elementov: Izberite element, ki se pojavi samo v posamezni molekuli reaktanta in samo v posamezni molekuli izdelka. To pomeni, da boste morali najprej uravnotežiti ogljikove atome.
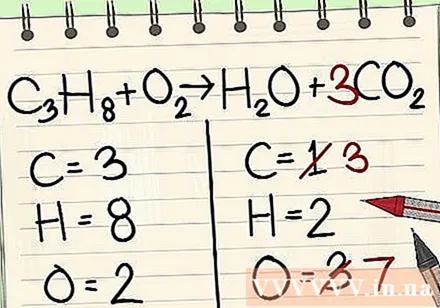
Dodajte koeficient za posamezne atome ogljika na desno stran enačbe, da jo uravnotežite s tremi atomi ogljika na levi strani enačbe.- C3H8 + O2 -> H2O + 3CO2
- Faktor 3 pred ogljikom na desni strani kaže, da obstajajo 3 atomi ogljika, kot sub-3 na levi pa 3 atome ogljika.
- V kemijski enačbi lahko spremenite koeficient, ne pa tudi indeksa.
Sledi atomska bilanca vodika. Na levi strani imate 8 atomov vodika. Zato boste potrebovali 8 na desni strani.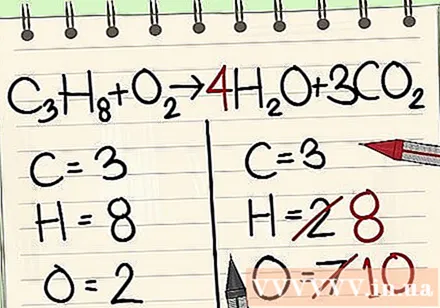
- C3H8 + O2 -> 4H2O + 3CO2
- Zdaj desno dodajte 4 kot faktor, ker spodnja številka kaže, da že imate 2 atoma vodika.
- Ko pomnožite faktor 4 z indeksom 2, dobite 8.
- Preostalih 6 atomov kisika je iz 3CO2. (3x2 = 6 atomov kisika + 4 drugi atomi kisika = 10)
Uravnotežite atome kisika.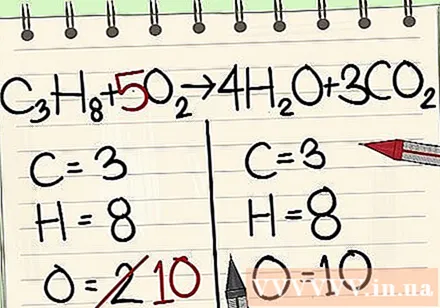
- Ker ste molekulam na desni strani enačbe dodali koeficiente, se je število atomov kisika spremenilo. Zdaj imate 4 molekule kisika v molekuli vode in 6 atomov kisika v molekuli ogljikovega dioksida. Skupaj imamo 10 atomov kisika.
- Faktor 5 dodajte molekuli kisika na levi strani enačbe. Zdaj imate na vsaki strani po 10 molekul kisika.
- C3H8 + 5O2 -> 4H2O + 3CO2.

- Atomi ogljika, vodika in kisika so v ravnovesju. Vaša enačba je končana.
Metoda 2 od 2: Ravnotežje po algebrski metodi
Enačbe zapišite po simbolih in formulah. Primer a = 1 in na podlagi te formule napiši enačbo.
Številke zamenjajte z njihovimi spremenljivkami.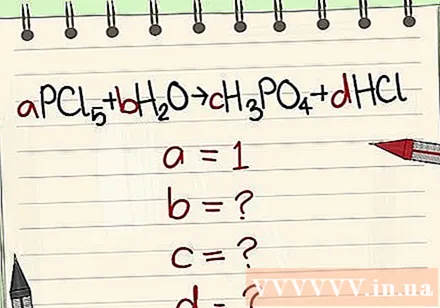
Preverite količino elementov v reaktorju in na strani izdelka.
- Primer: aPCl5 + bH2O = cH3PO4 + dHCl, tako da je a = 1 b = c = d = in ločitev elementov P, Cl, H, O, tako da dobite a = 1 b = 4 c = 1 d = 5 .
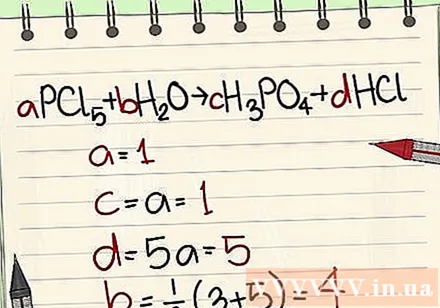
- Primer: aPCl5 + bH2O = cH3PO4 + dHCl, tako da je a = 1 b = c = d = in ločitev elementov P, Cl, H, O, tako da dobite a = 1 b = 4 c = 1 d = 5 .
Nasvet
- Ne pozabite poenostaviti enačbe.
- Če imate težave, lahko v orodje za spletno ravnotežje vnesete enačbo, da jo uravnotežite. Ne pozabite, da ob opravljanju izpita nimate dostopa do spletnega stanja, zato ne bodite odvisni od njega.
Opozorilo
- Nikoli ne uporabljajte koeficienta kot ulomka v kemijski enačbi - v kemijski reakciji ne morete deliti molekul ali atomov.
- Med ravnotežnim postopkom lahko uporabljate ulomke, vendar enačba ne bo uravnotežena, če so koeficienti še vedno ulomki.
- Če želite odstraniti ulomke, pomnožite celotno enačbo (levo in desno) z imenovalcem ulomka.